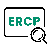Join us you will be able to get the following rights
Get fresh academic and clinical information
Sign up for exclusive endoscopy contests and training courses
Use online training software
Watch the LIVE of academic conferences and surgery
经典超声内镜病例:直肠癌术后局部复发
经典超声内镜病例:直肠癌术后局部复发
周春华 程桂莲 吴伟 徐丽明 吴永友 钟丰云 胡端敏
周春华(上海交通大学医学院附属瑞金医院消化科,原苏州大学附属第二医院消化科)
程桂莲 吴伟 徐丽明 胡端敏 (苏州大学附属第二医院消化科)
吴永友 钟丰云(苏州大学附属第二医院胃肠外科)
上篇小文介绍了直肠癌的EUS分期,本期主题为局部复发监测。文献报道,直肠癌术后的局部复发为5%-30%,因多数在浆膜侧,结肠镜很难早期发现。超声内镜可清晰显示直肠及周边盆腔结构,对浆膜侧的病灶敏感性高,故能早期诊断,从而获得根治性干预机会。本期内容,笔者围绕局部复发监测这一切入点,浅谈EUS的应用体会。
众所周知,直肠癌术后监测方法包括肛门指诊、血CEA、结肠镜、CT、MRI,甚至昂贵的PET-CT。既然有这么多的手段,还需要EUS吗?
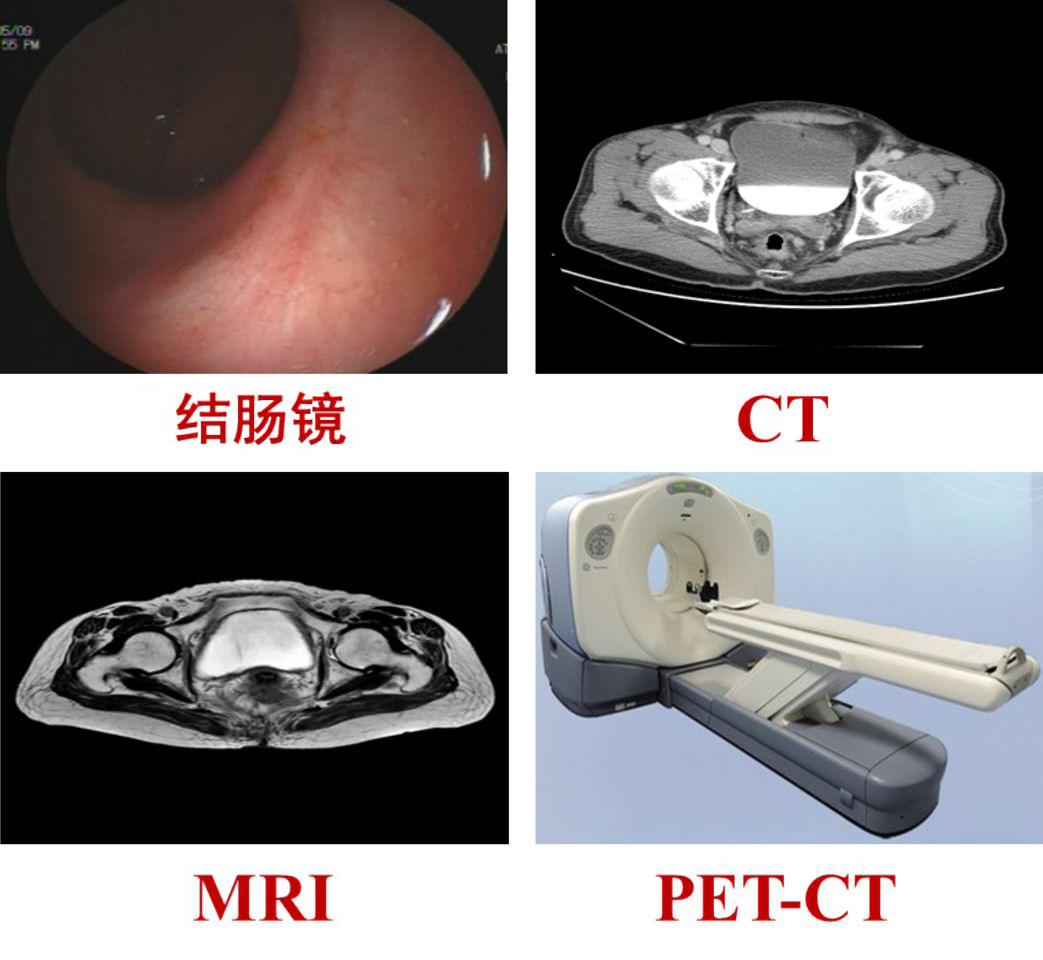
图1:临床上直肠癌术后监测的常用措施
首先,我们看看最新出炉的NCCN指南:⑴ 对于经肛局部切除者: 直肠镜(同时EUS或者增强MRI),前2年内每3-6月检查1次,然后5年内每6个月检查1次。⑵ 对于I期直肠癌:外科手术后,1年复查结肠镜,如果存在高危腺瘤,1年后复查,如果没有高危腺瘤,3年后复查,再5年后复查。⑶ 对于II-IV期直肠癌,措施包括:① 病史和体检:2年内每3-6个月1次,然后5年内每6个月1次;② 2年内每3-6个月检查CEA, 然后5年内每6个月1次;③ 胸/腹盆CT: II、III期病变,5年内每6-12个月1次;IV期病变,2年内每3-6个月1次,然后5年内每6-12个月1次。④ 术后1年内行结肠镜检查,如果术前因肿瘤梗阻无法行全结肠镜检,术后3-6个月复查;如果存在高危腺瘤,1年后复查,如果没有高危腺瘤,3年后复查,再5年后复查。⑤PET-CT 不推荐作为直肠癌术后常规监测手段(图2)。

图 2:2020年NCCN指南关于直肠癌术后监测
指南中对于EUS的价值比较谨慎,缺少一些前瞻性、对照性研究。评价一项诊断方法,主要是观察它的敏感性和特异性如何,以及阳性预测值、阴性预测值,如果两者均高,说明它的准确性高。结合我们的初步实践,发现EUS在直肠肿瘤术后复发监测中具有较好的敏感性和特异性。
(一)吻合口的EUS图像
EUS除了观察吻合口粘膜面,不同于正常直肠结构,超声图像还能显示高回声吻合钉,这有助于定位吻合的浆膜侧(图3B)。此外,我们还可观察手术区域是否存在肿大淋巴结。
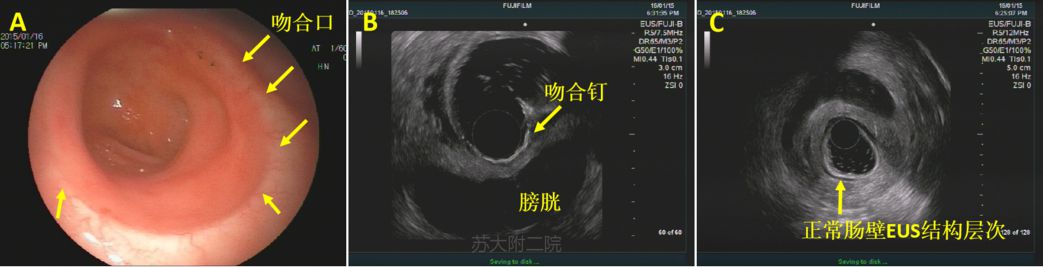
图3:直肠术吻合口处EUS图像
(二)EUS确诊直肠癌术后复发(敏感性)
随着外科手术和放、化疗方法的快速进展,直肠癌术后复发已明显减少,但及时发现仍有重要临床意义,接下来,通过几个病例介绍EUS的价值。
病例1:中年女性,因“直肠癌术后1年余,肛周不适近1月”入院。患者一年前确诊直肠癌于外院行 “直肠癌根治术(Dixon术)”,术后病理:溃疡型腺癌,分化Ⅱ-Ⅲ级,癌组织浸润肠壁全层及周围脂肪组织,神经束见癌累及(pT3N0M0- IIA 期)。术后行XELOX方案化疗六次。查体:直肠指检示吻合口左后方可及一质硬肿物,活动度尚可,无压痛,直径约1.5-2.0cm,指套无染血。血CEA正常。患者外院行结肠镜检查及CT检查均提示未见吻合口复发、转移(图4),遂来我科就诊。
EUS可见局部吻合口光滑(图5A),Radial 超声内镜提示固有肌层不均匀低回声肿块(图5B),考虑局部复发,进行穿刺(图5C),病理提示腺癌(图5D)。后患者行腹会阴联合直肠癌切除术+乙状结肠永久性造口术,术后大体病理提示 :(直肠)中分化腺癌,结合病史考虑复发,浸润深肌层,直肠、肛门切缘未见癌累及(图6)。
 图4:CT报告
图4:CT报告
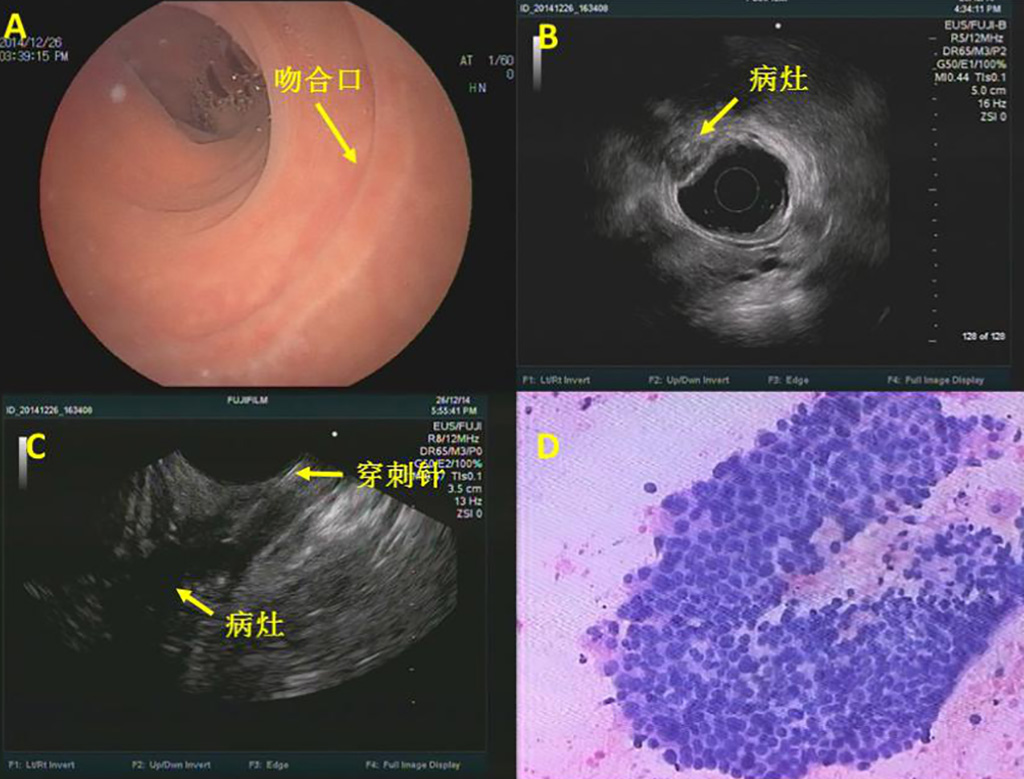
图5:EUS图像及穿刺病理
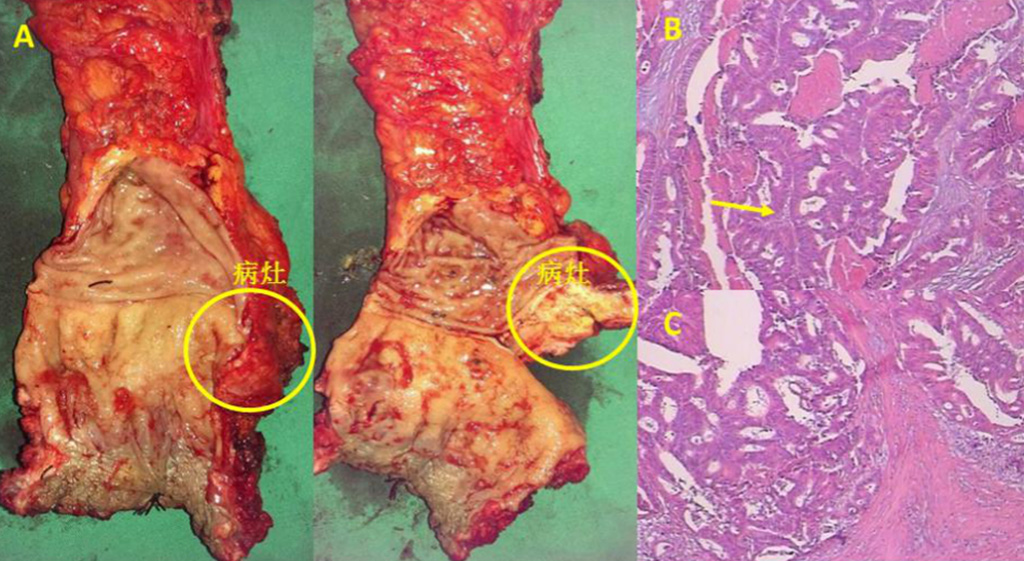
图6:大体病理及HE染色
病例2:老年男性,因直肠增生灶行经肛内镜微创手术(Transanal Endoscopic Microsurgery, TEM)治疗,术后病理提示:(直肠)腺瘤,局部高级别上皮内瘤变伴癌变,侵及粘膜下层,切缘未累及。建议追加手术,因无法保留肛门,患者拒绝,后密切随访。术后3个月第一次复查肠镜见疤痕,病理提示:急慢性炎及炎性肉芽组织增生。术后6个月第二次复查结肠镜仍见疤痕(图7A和B)。病理:慢性炎,部分上皮轻度异型增生。复查CT和MRI示直肠Ca术后改变,直肠中上段肠壁增厚。患者血CEA水平正常。EUS检查提示:直肠壁内可见不规则、不均匀低回声结节,累及固有肌层、浆膜层,凸向腔外(图7C和D)。FNA病理可见癌细胞(图7 E)。后患者再行根治术,术后病理提示:(直肠)粘液腺癌(图7 F)。
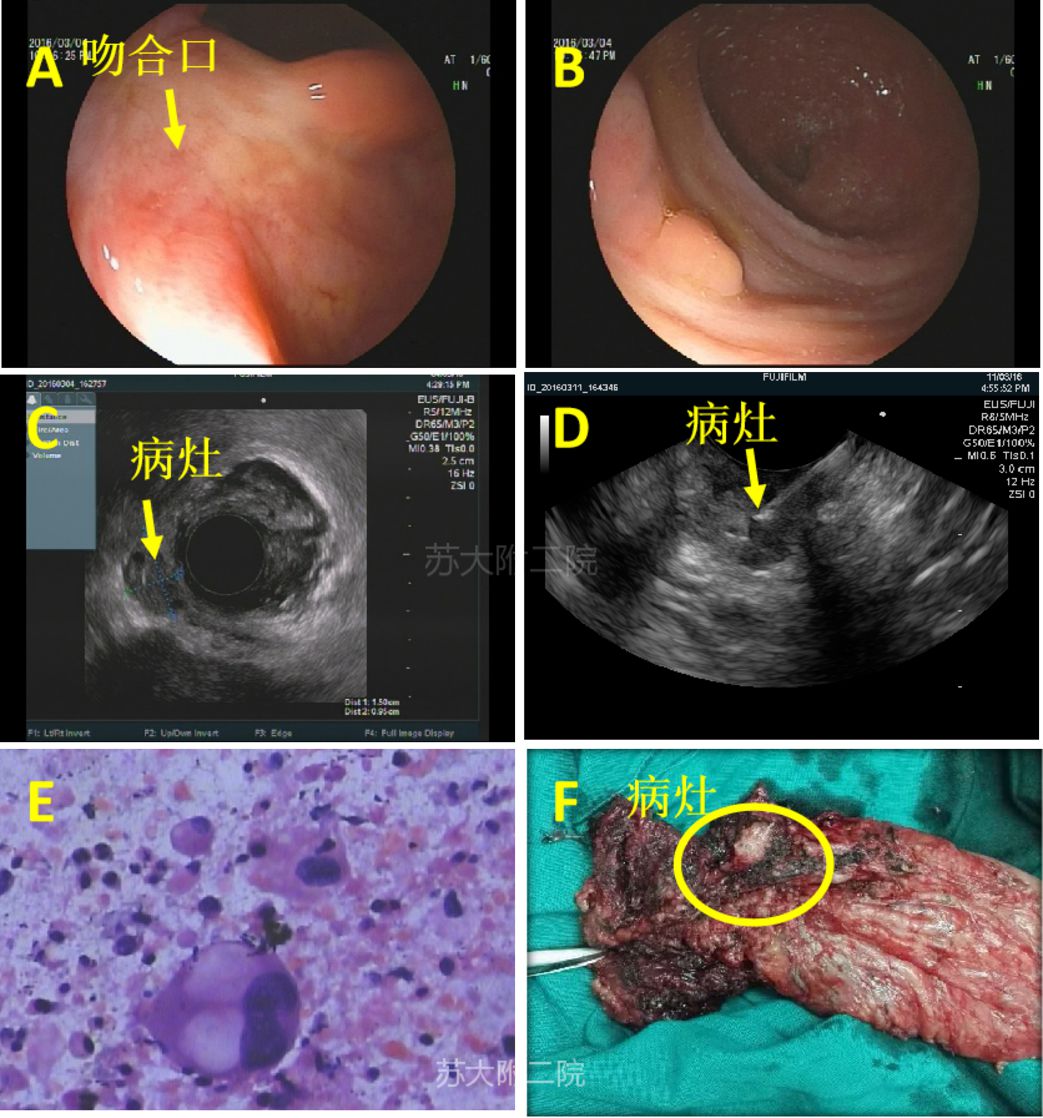
图7:结肠镜、EUS、FNA、手术标本图
病例3:老年女性,三年前因直肠肿物行经肛内镜微创手术(Transanal Endoscopic Microsurgery, TEM),术后病理,绒毛状管状腺瘤,局部癌变(中分化),侵及粘膜下层,切缘未累及。患者拒绝追加手术,术后每6-12月复查肠镜,CT,MRI。三年后复查肠镜见直肠疤痕下方隆起(图8A),EUS探查见直肠壁内不均匀低回声结节,凸向腔外(图8B和C)。FNA病理见大量粘液中散在异性细胞团,考虑肿瘤复发(图8D),同期MRI可见粘膜下方的多囊性病灶(图8E),后患者再行根治术,术后病理提示粘液腺癌(图8 F)。
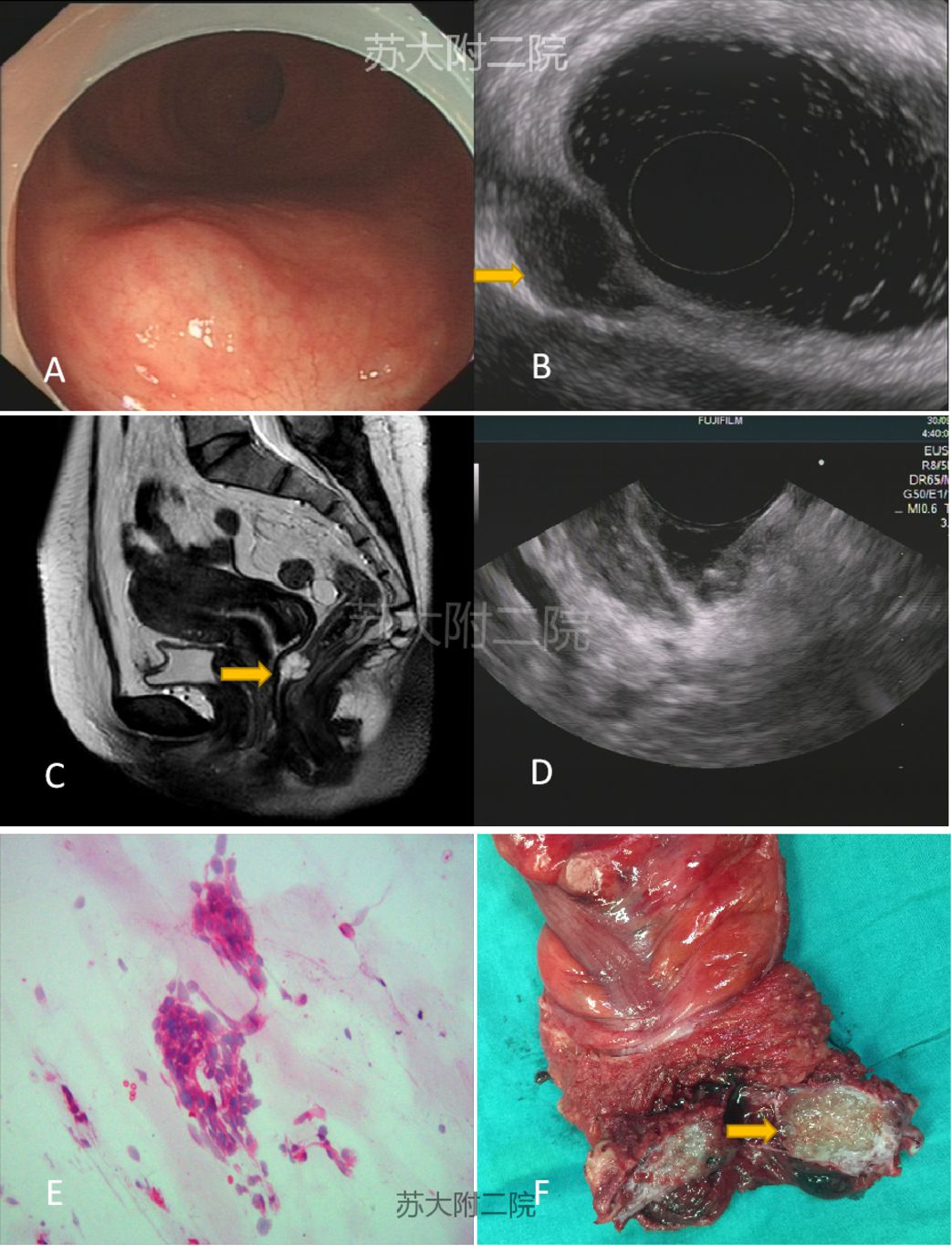
图8 A:肠镜见疤痕处隆起B:EUS见直肠壁凸向腔外结节(黄箭头)C: 盆腔MRI见直肠前壁囊性灶(黄箭头) D: EUS-FNA E: 大量粘液中散在异性细胞团 F:大体标本(黄箭头示粘液腺癌)
病例4:老年女性,2年前在外院因直肠息肉样病变行肠镜下切除手术,术后病理具体不详,来我院结肠镜检查发现直肠粘膜下隆起,表面光滑,EUS发现浆膜侧病灶,术后病理中分化腺癌,侵及全层,但粘膜面未累及,故为浆膜侧生长(图9)。

图9 A:肠镜见粘膜下隆起 B:EUS见直肠壁凸向腔外结节 C: 病理提示中分化腺癌(粘膜面未累及)
关于EUS对直肠癌术后复发的敏感性,国内也有文献报道,文中EUS确诊的两例患者,临床症状、结肠镜、CT检查均未发现异常,提示EUS具有较高的敏感性 (图10)。
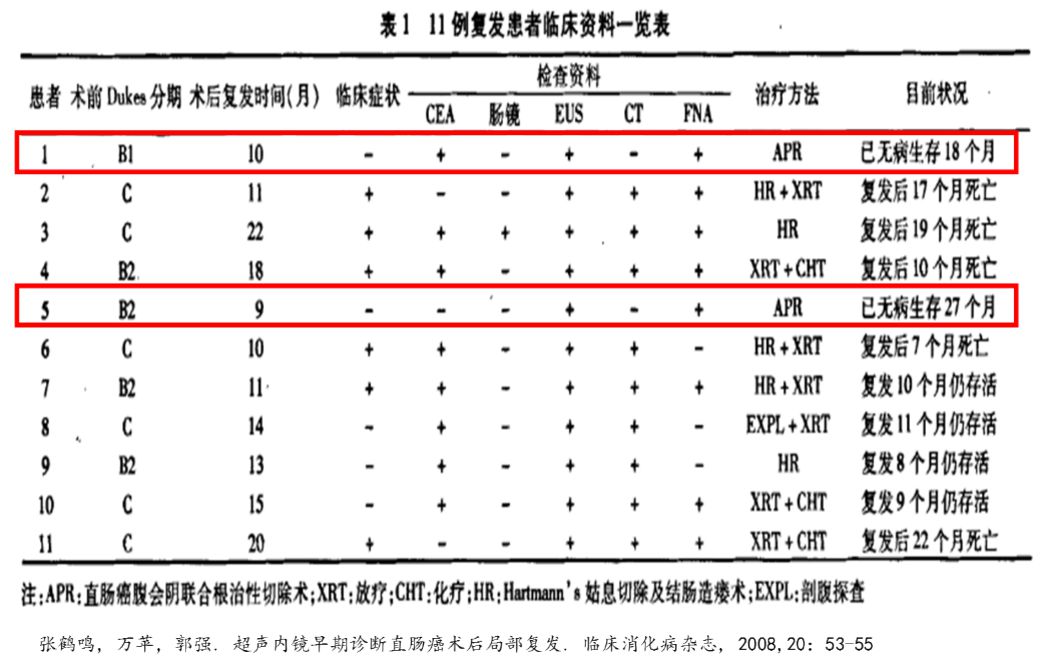
图10:超声内镜早期诊断直肠癌术后局部复发
(三)EUS排除直肠癌术后局部复发(特异性)
以上病例和文献均提示EUS有助于术后复发的早期诊断(高敏感性),现实工作中,我们发现EUS同样具有较好的特异性(排除复发),一起看看以下经典病例。
病例5:中年女性,因便血肠镜提示直肠腺癌,行Dixons手术。术后病理提示:中分化腺癌,侵及肌层,标本两切端未见癌累及,术后行3周期FOLFOX方案化疗及放化疗,半年后复查CT提示局部肠壁增厚,复发可能(图11A),EUS见吻合口光滑,肠壁层次结构清楚(图11 B和C),排除复发,随访证实。患者采用了储袋式直肠和乙状结肠吻合,致使盆腔存在较多对接肠管(图11 B),此外,放射性肠炎也导致肠壁水肿增厚,这些都增加了传统影像学对复发判断,但EUS通过注水延展肠壁,减少干扰因素,故排除复发更为自信。
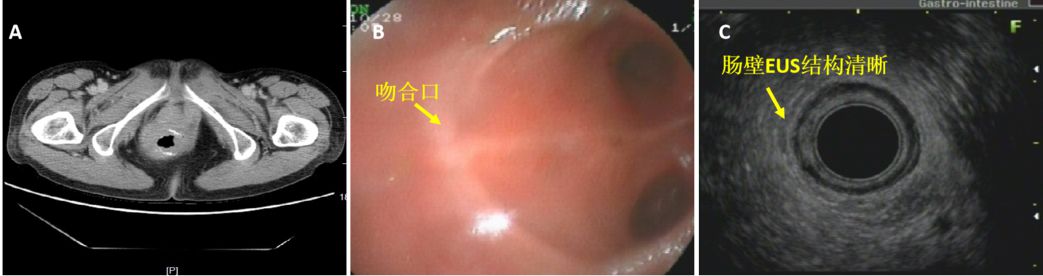
图11:CT及EUS图像
病例6:中年男性,因直肠腺癌外院手术,一年后肠镜复查见吻合口粘膜下隆起,考虑复发。EUS内镜视野见吻合口光滑隆起,旁边小开口(图12A-B),注水后粪水样物涌出(图12D和视频1),超声图像下吻合口外侧憩室,内可见混合回声(图12 C),故考虑憩室内粪石潴留,排除复发,后内镜手术证实(图12E-H)。
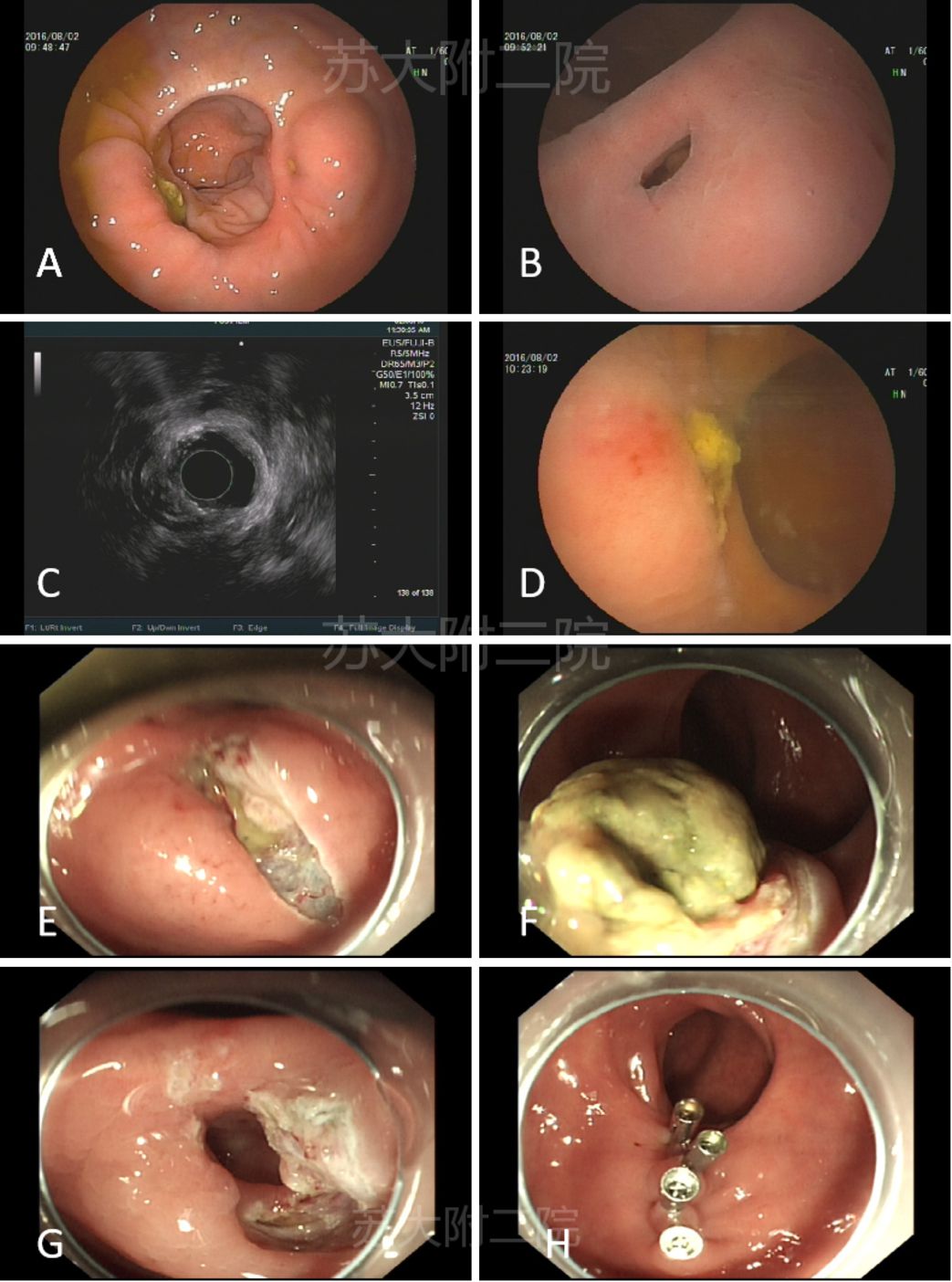
图12:吻合口憩室
视频1
病例7:老年男性,因直肠腺癌手术,两年后肠镜复查见吻合口粘膜下隆起,考虑复发。EUS内镜视野见吻合口光滑隆起,超声图像下吻合口外侧低回声囊肿(图 13 A和B),考虑术后吻合口种植性囊肿,MRI同时证实(图13 C)。
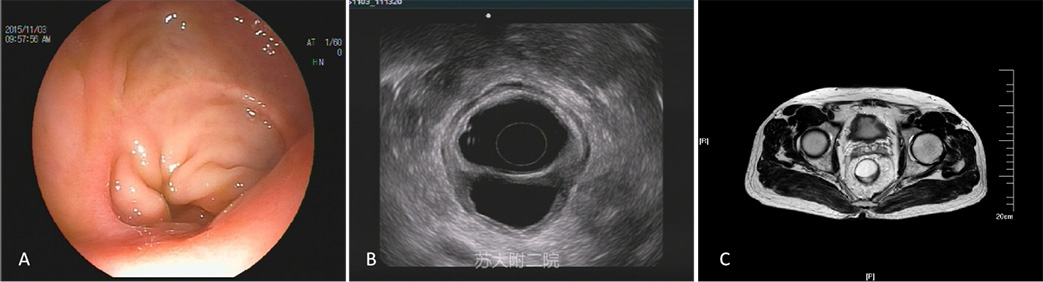
图13:吻合口种植性囊肿
EUS在直肠癌术后监测中的价值,国外研究也很少,早年的一项结果显示,相对于CT而言,EUS及引导下细针穿刺有极高的敏感性和特异性 (93%和91%)(图14)。

图 14 数据引用自Hünerbein M et al. The role of transrectal ultrasound-guided biopsy in the postoperative follow-up of patients with rectal cancer. Surgery. 2001 Feb;129(2):164-9.
综上,EUS能有效排除局部复发,具有高特异型。究其原因,可能是EUS检查时,先注水充分延展直肠,从而规避了肠腔塌陷、肠管堆积产生的干扰,故评估更客观、准确。下左图是小时候玩的猜中指游戏,当五个指头捏在一起时(相当于术后各段肠管堆积于盆腔),我们很难判断哪一根是中指(CT/MRI检查时),而当我们张开手掌,则十分容易(类似EUS检查时,注水延展肠壁)(图15)。
图15
(四)EUS对明确术后盆腔淋巴结转移的价值
直肠肿瘤术后,盆腔肿大淋巴结并不罕见,可以是炎症、术后放疗或转移所致。通常只能密切随访,但EUS-FNA是鉴别良、恶性淋巴结有效工具。
病例8:老年女性,外院肠镜检查示:直肠息肉样新生物。活检病理示:神经内分泌肿瘤,同时CT示肝左外叶低密度灶,考虑转移灶。行“肝左外叶切除术”和“直肠肿物切除术”。术后病理示:(肝脏)实转移性神经内分泌癌,中度分化,结合临床考虑来自直肠。(直肠)神经内分泌瘤 G2。术后化疗六次。术后密切随访,CT发现直肠周边淋巴结较前增大(图16),考虑转移。故EUS探查:吻合口未见异常,周边看见一0.7cm类圆形低回声灶,予以更换线阵EUS穿刺(图17A和B),病理提示:(盆腔淋巴结穿刺组织)见少量小圆细胞,IHC 示:LCA(-)、Syn(+)、CD56(+),考虑小圆细胞恶性肿瘤(NET)(图17 C和D)。
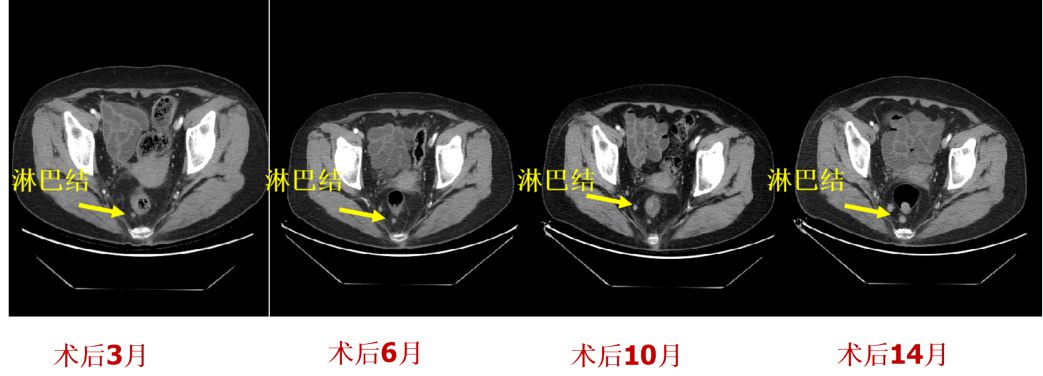
图16:CT复查随访图像
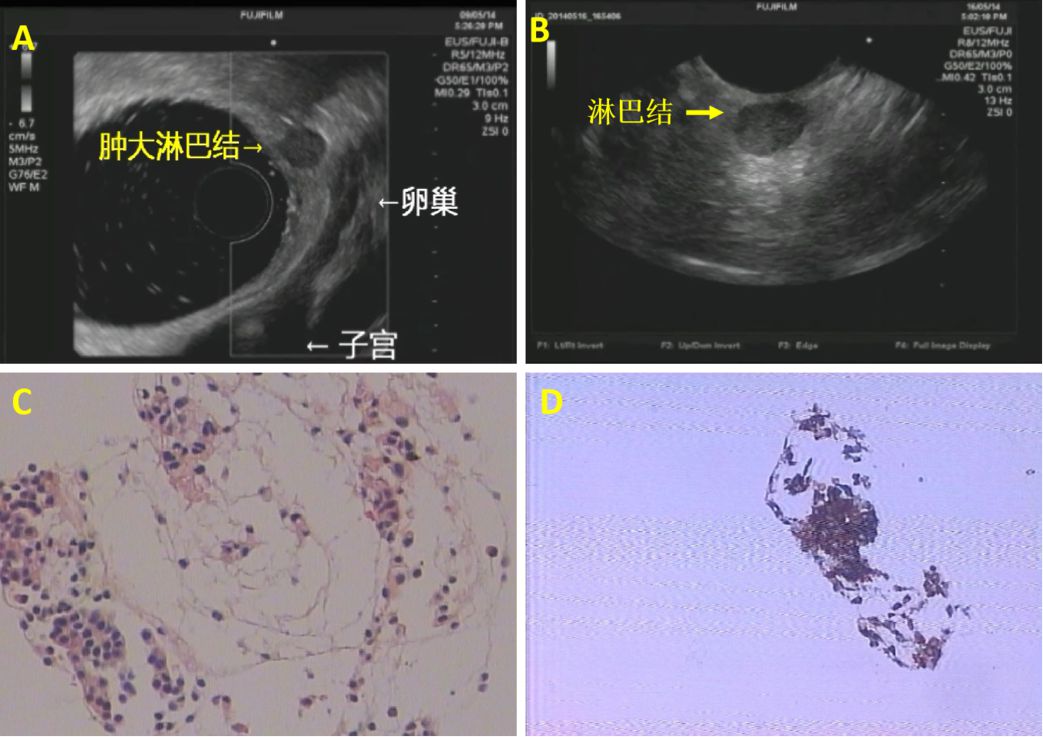
图17:EUS图像及FNA病理图
视频2
直肠癌术后监测,强调多种手段配合,依指南规范进行,EUS术者要积极参与到多学科团队中,这样不仅在临床上、学术上得到提高,也为患者真正带来益处。笔者认为EUS能够注水将肠腔充盈,能更清晰地观察到肠壁各个层次结构及周围组织情况,故对早期发现复发有较高价值,但尚需大样本的临床研究证实。本期内容是猪年的最后一次推送,预祝各位读者鼠年快乐,也期待EUS盆腔探查的最后一期---直肠周围病变和大家见面。
声明
富士胶片内镜世界(LIFE World)所登载的内容及其版权和使用权归作者本人与富士胶片所有。如发现会员擅自复制、更改、公开发表或其他以盈利为目的的使用,富士胶片将追究其法律责任。网站信息中涉及的治疗手技皆为术者个人针对该名患者特定体质及健康状况所采取的手法;术者对器械和药品种类的选择,也受到手术发生时间、地点等诸多因素的影响。因而相关内容及信息仅供会员参考。如盲目使用网站信息中涉及的治疗手技而发生意外,恕富士胶片及本网站对此不承担任何责任。

推荐内容
-
下消2025/02/14超声内镜经典病例之:下消化道皮革病“皮革胃”对消化科医生而言并不罕见,它1854年由Brinton提出,是弥漫性或浸润性胃癌形态学上的一种表现,组织学上均为低分化/印戒细胞,伴纤维化和结缔组织增生,呈现很强的促结缔组织增生反应,胃壁形同“皮革”,故得名。虽然该形态多见于胃,但不限于胃。据文献报道,皮革病变可发生膀胱、胆囊、结直肠等任何空腔脏器(图1)。
-
下消2024/10/16经典超声内镜病例:“恶魔之眼”消化道粘膜下肿瘤(Submucosal Tumor SMT)的内镜切除已日益普及,然而时有“假SMT”被误切的报道,其中外压或粘膜下变异血管无疑是最凶险的“假瘤子”,稍有不甚将酿成大祸,将这些貌似SMT的血管称之为“内镜切除之地雷”毫不为过。我们团队曾撰文详细介绍过上消化道血管性外压的形态和分布,本期微文将介绍另外一种凶险的“假瘤子”-----黏膜下畸形动脉。
-
下消2021/04/07经典超声内镜病例:结直肠多发黏膜下隆起提到结、直肠的单个黏膜下隆起,首先想到的应该是脂肪瘤、囊肿、类癌等常见病,但弥漫分布,多发黏膜下病灶呢?估计一时很难对号入座,这一期经典病例分享给大家的就是这一组少见的肠道改变。
-
下消2020/09/16经典超声内镜病例:超声世界里的“牛魔王”和“皮卡丘”医学影像里,为方便记忆和鉴别诊断,常采用熟识事物类比疾病的特征表现,比如用于诊断贲门失弛缓的“鸟嘴”。同样、EUS世界也很多相同情况,像今天要给大家带来的“皮卡丘”---肠道子宫内膜异位症。
-
下消2020/03/04经典超声内镜病例:直肠周边及盆腔病变如果上一期主题(超链接)是EUS的小众应用,那么今天内容则可为跨界适应症-------直肠周边及盆腔病变。超声内镜主要用于消化系统,但操作时不可避免地探查到其他系统(如泌尿和生殖),虽然这些脏器不期而遇,我们也无意“越俎代庖”,但熟悉它们的解剖位置和超声特点对快速定位,鉴别诊断帮助巨大。因此笔者认为,一个优秀的EUS术者不应忽视见到的任何EUS图像,要尽可能用已有解剖知识去解析你的图像,当按以上原则践行和指导操作,你最终意识到,原来EUS还有如此强大的功能(比如:超链接,肾上腺探查)。接下来我们一起看看盆腔系列的第三期内容吧。
-
下消2019/12/27经典超声内镜病例:盆腔探查策略及直肠癌分期当下,超声内镜(EUS)主要用于上消化道及胆、胰探查。对于直肠及盆腔病变,仅作为其他影像工具(如CT和MRI)的补充。但就我们的经验而言,EUS不仅直视肠腔、还能注水延展肠壁,对直肠癌的分期、浆膜侧复发等有一定优势。